据报道,每年约有年产量30%的钢铁遭腐蚀(主要是电化学腐蚀),我国每年因材料腐蚀破坏造成的经济损失高达数千亿元。
金属腐蚀是金属材料因环境因素(例如水分、氧气、化学物质等)作用而逐渐破坏和损耗的过程。
均匀腐蚀:金属表面均匀受损,腐蚀程度在整个表面上较为一致。点蚀:在金属表面形成局部的小洞,常在不锈钢等合金材料中见。缝隙腐蚀:在金属与金属或与非金属的接触界面形成的狭窄缝隙中发生的局部腐蚀。应力腐蚀开裂:金属在受到拉伸应力和特定腐蚀介质的双重作用下发生的裂纹,进一步导致破坏。晶间腐蚀:集中在晶界区域的腐蚀,容易导致材料断裂。选择性腐蚀:合金中的某种元素比其他元素更容易腐蚀,导致组成发生变化。按照发生化学反应的类型,可以分为化学腐蚀和电化学腐蚀。金属表面与介质(如气体或非电解质液体等)因发生化学作用而引起的腐蚀,称为化学腐蚀。化学腐蚀作用进行时无电流产生。金属表面与介质(如潮湿空气或电解质溶液等)因形成微电池,金属作为阳极发生氧化而使金属发生腐蚀,这种由于电化学作用引起的腐蚀称为电化学腐蚀。当两种金属或者不同的金属制成的物体相接触时,同时又与其它介质相接触时,就形成了一个原电池,并进行原电池的电化学作用。带有铁铆钉的铜板若暴露在空气中,表面被潮湿空气或雨水浸润,空气中的CO2、SO2和海边空气中的NaCl溶解其中,形成电解质溶液,铜作阴极,铁作阳极,这样组成了原电池。

二价铁被空气中的氧气氧化成三价铁,三价铁在水溶液中生成氢氧化铁沉淀, 氢氧化铁 又可能部分失水生成三氧化二铁 。所以铁锈是一个由二价铁、三价铁、氢氧化铁、三氧化二铁等化合物组成的疏松的混杂物质。

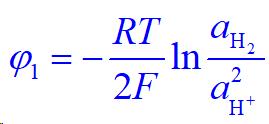
在酸性气氛中,大气中的氧气在阴极上获得电子,发生还原反应(亦称为吸氧腐蚀)


含有杂质的金属表面,由于金属和杂质的电势的差异,容易构成以金属和杂质为电极的许多微电池(或局部电池)。氢离子在铁阴极上放电,锌作为阳极不断溶解而受到腐蚀。所以,含有铁杂质的粗锌在酸性溶液中,既有化学腐蚀,又有电化学腐蚀,要比纯锌腐蚀得更快。
涂层保护:涂上绝缘的油漆或塑料等非金属层,隔绝金属与腐蚀介质的接触。
电镀:在金属表面镀上一层不易腐蚀的金属,如镀锌、镀铬等。
热喷涂:将金属或非金属材料以高温形式喷涂到金属表面形成保护层。
阴极保护:通过外加直流电源,使受保护金属作为阴极,并牺牲另一易腐蚀的金属作为阳极。
制成耐蚀合金
在炼制金属时加入其他组分,提高耐蚀能力。
如在炼钢时加入Mn,Cr等元素制成不锈钢。
阳极保护:将金属表面氧化,形成密封的氧化膜,阻止进一步腐蚀。
化学抑制剂:添加到环境中的化学物质,减缓腐蚀速度或阻止特定腐蚀反应。
设计控制:改善结构设计,避免产生容易腐蚀的死角,缝隙和接触腐蚀敏感区。
环境控制:控制或改善金属周围的环境,如调节湿度,温度,避免有害化学物质的接触。
为了保护金属材料,通常会结合多种防腐方法来提高防护效果。金属防腐蚀技术在船舶、管道、建筑、汽车制造以及石油化工等诸多领域皆有重要应用。